O Ministério da Agricultura e Pecuária (Mapa) iniciou um período de consulta pública, com duração de 45 dias, focando na minuta da Portaria 1.590/2026. O objetivo principal desta medida é estabelecer um regulamento técnico detalhado para o registro de medicamentos genéricos e de produtos similares intercambiáveis destinados ao uso veterinário no Brasil. Essa iniciativa visa aprimorar a legislação existente, garantindo maior segurança e eficácia nos fármacos utilizados em animais.
A iniciativa do Mapa representa um passo significativo para a modernização das normas que regem o setor de saúde animal. A abertura da chamada para contribuições tem a finalidade de coletar sugestões, esclarecimentos e propostas de melhorias do público, de especialistas e da indústria, que serão cruciais para a formulação da futura legislação. Este processo colaborativo busca assegurar que o texto final da portaria seja abrangente e reflita as necessidades e os avanços técnicos da área.
Consulta Pública: Mapa Discute Genéricos Veterinários
Para participar da consulta pública sobre os medicamentos veterinários, os interessados devem encaminhar suas sugestões de forma tecnicamente fundamentada. O envio das contribuições é realizado por meio do Sistema de Monitoramento de Atos Normativos (Sisman), ferramenta gerida pela Secretaria de Defesa Agropecuária do próprio Mapa. É imprescindível que os participantes realizem um cadastro prévio na plataforma “Solicita” para terem acesso e poderem submeter suas propostas.
Definições Cruciais na Nova Portaria
A minuta da portaria em debate introduz e esclarece importantes distinções entre as diferentes categorias de medicamentos de uso veterinário, conceitos que são fundamentais para a regulamentação:
- Medicamento de Referência: Trata-se do produto farmacêutico devidamente registrado no Ministério da Agricultura e Pecuária, cuja eficácia e segurança foram cientificamente comprovadas, em conformidade com as exigências estabelecidas pelas normas vigentes. Ele serve como padrão para os demais.
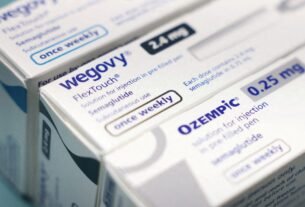
- Medicamento Genérico: Este tipo de medicamento é identificado exclusivamente pela Denominação Comum Brasileira (DCB) de seu princípio ativo. A regulamentação proíbe expressamente a utilização de qualquer nome comercial ou marca para esses produtos, visando simplificar a identificação e o acesso.
- Similar Intercambiável: Ao contrário do genérico, o similar intercambiável é identificado por um nome comercial específico. Seu registro é concedido com base em estudos de comparabilidade que atestam sua equivalência com um medicamento de referência, previamente indicado e reconhecido pelo Ministério da Agricultura e Pecuária. Não pode usar apenas a DCB ou DCI (Denominação Comum Internacional) como nome comercial.
Critérios para Equivalência Terapêutica e Bioequivalência
A Portaria detalha que a comprovação da equivalência terapêutica entre dois medicamentos será estabelecida quando ambos, sendo equivalentes farmacêuticos, demonstrarem a mesma eficácia, segurança e período de carência. Essa comprovação é válida quando administrados na mesma dose e pela mesma via de administração. Essa é uma medida fundamental para garantir que genéricos e similares ofereçam os mesmos resultados que os medicamentos de referência.
A verificação da bioequivalência ou da equivalência farmacêutica é um requisito rigoroso e deve ser realizada por um laboratório que possua o devido reconhecimento e certificação. Este processo assegura a qualidade e a confiabilidade dos medicamentos que serão disponibilizados no mercado veterinário, protegendo a saúde animal e a segurança alimentar.
Novas Regras para Compras Governamentais e Prescrições
As diretrizes propostas na minuta da Portaria 1.590/2026 estabelecem que as compras governamentais de medicamentos de uso veterinário, assim como as prescrições emitidas por médicos veterinários, deverão obrigatoriamente adotar a denominação genérica do princípio ativo (Denominação Comum Brasileira – DCB) ou, na ausência desta, a Denominação Comum Internacional (DCI). Essa padronização visa facilitar a identificação, o controle e a transparência no mercado.
No que tange às aquisições realizadas pelo governo, os medicamentos genéricos terão preferência sobre os demais produtos, desde que as condições de preço sejam equivalentes. Esta medida busca promover a economia de recursos públicos e incentivar a produção e o uso de genéricos. Para as prescrições da medicina veterinária, a inclusão do nome comercial ou da marca do medicamento permanecerá como uma opção, não sendo obrigatória.

Imagem: agenciabrasil.ebc.com.br
As empresas que atualmente comercializam produtos com nomes que utilizam a DCB/DCI, mas que não se enquadram como genéricos, terão um prazo de dois anos para efetuar a alteração de seu nome comercial e remover a denominação genérica da marca. Este período será contado a partir da data de publicação do texto final da portaria, concedendo tempo hábil para adaptação da indústria. Além disso, o Mapa exige que todas as embalagens dos medicamentos genéricos contenham, de forma clara e visível, a frase “Medicamento genérico de uso veterinário”.
Produtos Não Abrangidos pela Regulação
É importante destacar que a regulamentação proposta pela Portaria do Ministério da Agricultura, atualmente em consulta pública, não se aplica a uma série de produtos de uso veterinário específicos. Essa delimitação visa concentrar os esforços regulatórios nos medicamentos que necessitam de uma nova categorização e controle. Os produtos excluídos da abrangência da portaria são:
- Produtos biológicos;
- Fitoterápicos;
- Derivados do plasma e do sangue;
- Cosméticos veterinários;
- Produtos com fins diagnósticos;
- Radiofármacos;
- Gases medicinais.
Próximos Passos Após a Consulta
Concluída a fase de escuta da sociedade, o Ministério da Agricultura e Pecuária (Mapa) programou para o dia 29 de maio a etapa de consolidação, análise e resposta às contribuições que forem recebidas. O prazo exato para a finalização deste processo de análise e a definição das etapas subsequentes ainda será determinado pela pasta, mas a data inicial já demonstra o compromisso com a agilidade na tramitação da nova legislação. Para acompanhar o andamento dessas regulamentações, é fundamental consultar o Ministério da Agricultura e Pecuária (Mapa).
Confira também: Investir em Imóveis na Região dos Lagos
A discussão em torno da Portaria 1.590/2026 marca um momento crucial para o setor de saúde animal no Brasil. Ao definir critérios claros para genéricos e similares, o Mapa busca fortalecer a segurança, a eficácia e a acessibilidade dos tratamentos veterinários. Manter-se informado sobre essas mudanças é essencial para profissionais, empresas e tutores de animais. Continue acompanhando nossa editoria de Política para mais análises sobre as políticas públicas que impactam o país.
Crédito da imagem: Paulo Pinto/Agência Brasil